España:
Noviembre del 2018. Las calles se visten de otoño, el chocolate caliente triunfa en las cafeterías y un simpático resfriado se refugia en tus pulmones. Por suerte cuentas con la ayuda de dulces jarabes, mantas mágicas y nutritivas sopas. ¡Menos mal que no estás solo! Sin embargo, el único ejército que puede ganar esa batalla está en tu interior y se llama sistema inmunitario. ¿Qué haríamos sin él? ¿Qué sería de nosotros en invierno? Pues bien, esta situación la viven cada día los afectados por Inmunodeficiencia Combinada Grave.
Esta dolencia tan desconocida protagonizó por unos años una increíble historia de ciencia ficción en pleno planeta Tierra. En 1971 nació David Vetter, conocido como “el niño burbuja”. Se le llamó así porque literalmente vivió toda su vida encerrado en un habitáculo de plástico que lo mantenía aislado de microorganismos patógenos. Únicamente salió de ella en siete ocasiones y lo hizo protegido por un traje diseñado nada más y nada menos que por la NASA. A los doce años David Vetter fue sometido a un trasplante, la única esperanza para salir de su cautiverio. Todo salió bien durante los primeros meses, hasta que se descubrió que en el tejido donado, procedente de su hermana mayor, había partículas del virus Epstein-Barr, responsable de la mononucleosis. Esta infección, que para cualquier mortal puede ser terrible, resultó fatídica para David Vetter. Falleció sin haber tenido la oportunidad de respirar aire fresco ni tan solo una vez.

Pero, ¿qué le ocurría exactamente a David Vetter? La Enfermedad del Niño Burbuja o Inmunodeficiencia Combinada Grave (IDCG) es una enfermedad rara que afecta a uno de cada 50.000 nacidos vivo. Se caracteriza por la falta de linfocitos T periféricos funcionales y la incapacidad de producir anticuerpos. Esto significa que el ejército de defensa está mermado y además es ciego ante la mayoría de los patógenos. Pueden campar a sus anchas por el cuerpo y tienen barra libre para inducir infecciones y enfermedades. Además, los niños con IDCG pueden sufrir retraso del crecimiento y son más susceptibles a infecciones oportunistas como la varicela, mononucleosis infecciosas y hongos
A día de hoy conocemos mutaciones en 15 genes autosómicos diferentes relacionadas con la Inmunodeficiencia Combinada Grave, pero en la mayoría de los pacientes la causa se encuentra en el gen IL2GR, localizado en el cromosoma X. Este gen codifica para una pieza de la interleukina-2, un tipo de citoquina. Pero, ¿de qué estamos hablando exactamente? Las citoquinas son las moléculas que las células del sistema inmunitario producen para comunicarse. Recordemos que este sistema está dispersado por nuestro organismo, pero se encuentra principalmente en la sangre. A diferencia de otros tejidos las células del sistema inmunitario no están unidas físicamente unas con otras, por lo que hacen falta moléculas intermediarias que difundan por el medio extracelular para que se entiendan unas con otras. Las citoquinas en concreto son la familia de “palabras” que informan a las células inmaduras del sistema inmunitario de que tienen que crecer y diferenciarse en células especializadas. Son el “cómete toda la comida para ser grande y fuerte” o “tienes que estudiar mucho si quieres ser tan lista como tus hermanas mayores”.
Concretamente, las células que reciben interleukina-2 se transforman en linfocitos. Como los pacientes de Inmunodeficiencia Combinada Grave no tienen interleukina-2 funcional, ninguna célula inmadura tomará este camino. El déficit o la ausencia de linfocitos se denomina linfopenia, y es uno de los principales síntomas para detectar y diagnosticar a los niños con IDCG. También se puede determinar mediante un diagnóstico prenatal, pero lo cierto es que esta prueba no sólo suele realizarse cuando aparece un embarazo de riesgo. Reconocer la enfermedad cuanto antes es esencial para ofrecerles una vida de mayor calidad.
Los niños con IDCG nacen totalmente indefensos y desde el primer día de vida son dependientes de un tratamiento. Lo más común es la administración de inmunoglobulinas, anticuerpos que dan la voz de alarma a las células inmunitarias que sí funcionan si ocurre algún problema. Esta solución cubre la carencia de anticuerpos, pero simplemente es un parche, no ataca la raíz del problema. Sin embargo, hoy en día y gracias a los avances de la biomedicina existen dos alternativas muy prometedoras que proponen sanar definitivamente a estos pacientes.
La primera es una candidata a ser la cura definitiva: la terapia génica. Este tratamiento consiste en extraer las células madre del tejido dañado, en este caso células madre de la médula ósea. Este tejido se encuentra en el interior de los huesos y es nuestra fábrica de sangre. En el laboratorio estas células se corrigen, añadiendo el gen que tienen dañado, y se vuelven a implantar en el paciente. De esta manera el paciente se cura gracia a sus propias células. ¡Es fantástico! Pero esta historia es demasiado bonita para ser cierta ya que la terapia génica apenas está dando sus primeros pasos. Hay casos clínicos con resultados magníficos, pero también hay muchos pacientes que han desarrollado efectos secundarios como leucemias. Hace falta todavía mucha investigación para que la terapia génica sea un tratamiento seguro, pero todos los expertos coinciden en que algún día será una realidad.
Mientras tanto, tenemos una segunda alternativa muy efectiva: el trasplante de médula ósea. Esta intervención también es la solución para otras patologías como la leucemia. En este caso se eliminan esas células madre de las que antes hablábamos y se sustituyen por las de otra persona. Es una intervención relativamente sencilla, pero es muy, muy poco probable encontrar un donante histocompatible.
Pero, ¿qué significa eso de ser histocompatible? Nuestras células tienen unas “etiquetas” con nuestro nombre, proteínas de membrana que identifican esas células como propias. Sirven para que el sistema inmunitario pueda reconocer nuestras células y no las ataque. Si nuestras células mutan o son infectadas esa etiqueta también cambia, así nuestras defensas pueden detectar que algo les ocurre y eliminarlas.
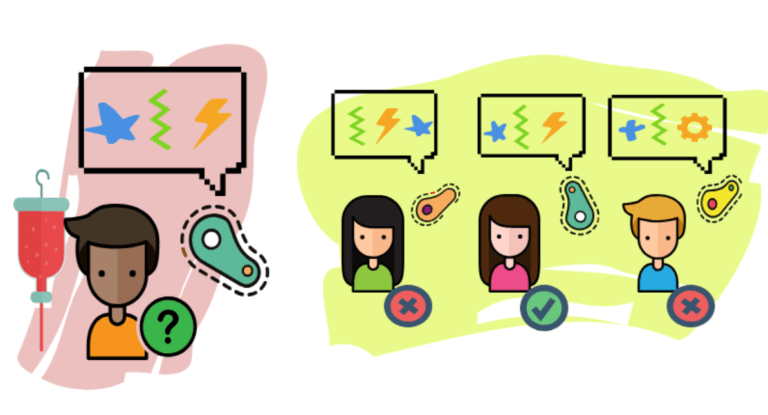
Pues bien, dos personas son histocompatibles cuando sus “etiquetas” son tan parecidas que no se pueden diferenciar. Lo más probable es que ocurra entre familiares cercanos, pero cuando no es así hay que recurrir a bancos de donación de médula que se construyen a partir de voluntarios anónimosEn España la Fundación Carreras creó en 1991 el Registro de Donantes de Médula Ósea (REDMO) con el objetivo de achacar la leucemia. Cuenta con más de 200.000 donantes voluntarios en España y tiene acceso a más de 27 millones por todo el mundo. Esto es muchísima gente, pero queda lejos de los 7 mil millones de personas que habitamos la Tierra. Entrar en el banco de donantes de médula ósea es muy sencillo, no cuesta dinero y puede que el día de mañana sirva para salvar una vida. Es muy importante tener claro que NO es una intervención que elimine la médula ósea del donante, y TAMPOCO imposibilita donar médula en el futuro a un familiar.
En cuanto a la intervención para extraer médula ósea tenemos dos posibilidades. Por un lado la recolección de médula ósea, que consiste en una punción de las crestas ilíacas (hueso de la cadera) para extraer directamente las células. No es peligrosa, aunque puede que en los días siguientes los analgésicos tengan trabajo con algunas molestias. El otro método es la aféresis, donde primero se administran unos fármacos que estimulan la salida de las células madre desde el interior de los huesos a todo el circuito sanguíneo y después se extrae la sangre, se filtra para separar las células que se quieren extraer y el resto de los componentes se devuelven al donante. Este mecanismo recuerda a la diálisis, dura un rato y no tiene grandes efectos secundarios. La forma de extracción de las células se valorará según las necesidades del paciente y la opinión del donante.
Quizás un donante nunca coincida en sus años de vida con un paciente compatible pero si ocurre es importante comprender que formar parte del Registro de Donantes de Médula Ósea no significa que sea obligado donar. Además se realizan pruebas médicas para corroborar que la salud del donante es la adecuada para someterse a la donación. Sin embargo, si todo está correcto pero nos da miedo la intervención hay que tener en cuenta un detalle: lo que para el donante puede ser una intervención que asuste un poco, para el receptor es seguramente su única esperanza.
Hoy en día las personas diagnosticadas con Inmunodeficiencia Combinada Grave pueden llevar a cabo una vida “normal”. No las podemos reconocer por la calle, pero se estima que en Valencia son unas 16, 133 en Madrid y 140.000 en todo el mundo. Personas con inquietudes, aficiones y amigos. Muchas de estas personas necesitan recibir una médula ósea y quizás, sólo quizás, la esperanza se encuentra en su misma calle, país o planeta. La medicina nos ofrece soluciones directas para la mayoría de enfermedades, pero del mismo modo que el cariño de un amigo es único e irrepetible, a veces también lo es nuestra solidaridad.
Artículos relacionados: inmunodeficiencia combinada grave, enfermedades raras, cromosoma x
Autor: Elena Juan Andrés
Fuente: Genética Médica Blog https://goo.gl/jrnD3h









