Estados Unidos:
La Administración de Drogas y Alimentos de EE. UU. Aprobó hoy tabletas de Daurismo (glasdegib) para usarse en combinación con citarabina en dosis baja (LDAC), un tipo de quimioterapia, para el tratamiento de la leucemia mieloide aguda (LMA) recién diagnosticada en adultos de 75 años de edad o más o que tengan otras afecciones o enfermedades crónicas de salud (comorbilidades) que pueden impedir el uso de quimioterapia intensiva.
“La quimioterapia intensiva generalmente se usa para controlar la AML, pero muchos adultos con AML no pueden recibir quimioterapia intensiva debido a sus efectos tóxicos. La aprobación de hoy brinda a los proveedores de atención médica otra herramienta para usar en el tratamiento de pacientes con AML con diversas necesidades únicas. «Los ensayos clínicos mostraron que la supervivencia general mejoró con el uso de Daurismo en combinación con LDAC en comparación con LDAC solo para pacientes que no tolerarían la quimioterapia intensiva», dijo Richard Pazdur, MD, director del Centro de Excelencia Oncológica de la FDA y director interino de la Oficina de Hematología y productos de oncología en el Centro de Evaluación e Investigación de Medicamentos de la FDA.
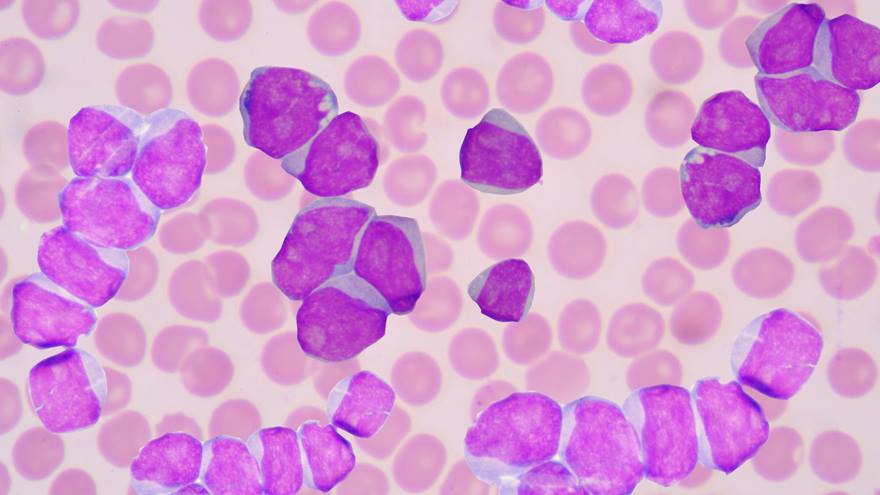
La AML es un cáncer que progresa rápidamente y se forma en la médula ósea y produce un aumento en el número de glóbulos blancos anormales en el torrente sanguíneo y en la médula ósea. El Instituto Nacional del Cáncer en los Institutos Nacionales de la Salud estima que en 2018, aproximadamente 19,520 personas serán diagnosticadas con AML y aproximadamente 10,670 pacientes con AML morirán de la enfermedad. Casi la mitad de los adultos diagnosticados con AML no son tratados con quimioterapia intensiva debido a comorbilidades y toxicidades relacionadas con la quimioterapia.
La eficacia de Daurismo se estudió en un ensayo clínico aleatorizado en el que 111 pacientes adultos con AML recién diagnosticados fueron tratados con Daurismo en combinación con LDAC o LDAC solo. El ensayo midió la supervivencia general (SG) desde la fecha de la aleatorización hasta la muerte por cualquier causa. Los resultados demostraron una mejora significativa en la SG en pacientes tratados con Daurismo. La mediana de SG fue de 8,3 meses para los pacientes tratados con Daurismo más LDAC, en comparación con 4,3 meses para los pacientes tratados con LDAC solamente.
Los efectos secundarios comunes informados por los pacientes que reciben Daurismo en ensayos clínicos incluyen recuento bajo de glóbulos rojos (anemia), cansancio (fatiga), hemorragia (hemorragia), fiebre con bajo recuento de glóbulos blancos (neutropenia febril), dolor muscular, náuseas, hinchazón de brazos o piernas (edema), recuento plaquetario bajo (trombocitopenia), dificultad para respirar (disnea), disminución del apetito, sabor distorsionado (disgeusia), dolor o llagas en la boca o garganta (mucositis), estreñimiento y erupción cutánea.La FDA otorgó la aprobación de Daurismo a Pfizer.Los efectos secundarios comunes informados por los pacientes que reciben Daurismo en ensayos clínicos incluyen recuento bajo de glóbulos rojos (anemia), cansancio (fatiga), hemorragia (hemorragia), fiebre con bajo recuento de glóbulos blancos (neutropenia febril), dolor muscular, náuseas, hinchazón de brazos o piernas (edema), recuento plaquetario bajo (trombocitopenia), dificultad para respirar (disnea), disminución del apetito, sabor distorsionado (disgeusia), dolor o llagas en la boca o garganta (mucositis), estreñimiento y erupción cutánea.
La información de prescripción para Daurismo incluye una Advertencia en caja para asesorar a los profesionales de la salud y los pacientes sobre el riesgo de muerte embrionaria o defectos congénitos graves. Daurismo no debe utilizarse durante el embarazo o durante la lactancia. Las pruebas de embarazo se deben realizar en mujeres en edad reproductiva antes de iniciar el tratamiento con Daurismo y se debe usar un método anticonceptivo eficaz durante el tratamiento y durante al menos 30 días después de la última dosis. La Advertencia en el recuadro también informa a los pacientes masculinos sobre el riesgo potencial de exposición al medicamento a través del semen y el uso de condones con una pareja embarazada o una mujer que pueda quedar embarazada tanto durante el tratamiento como al menos 30 días después de la última dosis. Daurismo debe ser dispensado con una Guía de medicamentos para el paciente que describa información importante sobre los usos y riesgos de la droga. También se debe recomendar a los pacientes que no donen sangre ni hemoderivados durante el tratamiento. Los proveedores de atención médica también deben monitorear a los pacientes para detectar cambios en la actividad eléctrica del corazón, llamada prolongación QT.
La FDA otorgó a esta solicitud la designación de revisión prioritaria. Daurismo también recibió la designación de medicamento huérfano, que ofrece incentivos para ayudar y alentar el desarrollo de medicamentos para enfermedades raras.
La FDA otorgó la aprobación de Daurismo a Pfizer.
La FDA, una agencia dentro del Departamento de Salud y Servicios Humanos de los Estados Unidos, protege la salud pública al garantizar la seguridad, la eficacia y la seguridad de los medicamentos humanos y veterinarios, las vacunas y otros productos biológicos para uso humano y los dispositivos médicos. La agencia también es responsable de la seguridad y protección del suministro de alimentos, cosméticos, suplementos dietéticos, productos que emiten radiación electrónica de nuestra nación y de la regulación de los productos de tabaco.
Artículos relacionados: leucemia mieloide aguda, enfermedades raras, tratamiento
Fuente: https://goo.gl/H3Mruy