Sinónimos: Deficiencia ASA, Deficiencia ASL, Deficiencia de argininosuccinato liasa, Deficiencia de arginosuccinato, Deficiencia de ácido argininosuccínico liasa
Prevalencia: 1-9 / 100 000
Herencia: Autosómico recesivo
Edad de inicio o aparición: Neonatal, Cualquier edad
Definición de la enfermedad
La aciduria argininosuccínica (AAS) es un trastorno metabólico del ciclo de la urea. Se presenta frecuentemente como una forma grave de aparición neonatal, manifestándose en los primeros días de vida como hiperamonemia acompañada de vómitos, de hipotermia, de letargia y de dificultades para la toma del alimento, pudiendo conducir al coma y a la muerte. Alternativamente, puede manifestarse de forma tardía por hiperamonemia episódica inducida por las infecciones o el estrés, o, a veces, por alteraciones de la conducta y/o dificultades de aprendizaje. A menudo, los pacientes manifiestan disfunción hepátidica.
Resumen
Epidemiología
La prevalencia de la AAS en los Estados Unidos y en Europa se ha estimado en 1/218.750 nacidos vivos.
Descripción clínica
La AAS puede tener un cuadro clínico variable, sea de inicio neonatal o de inicio tardío (a cualquier edad fuera del período neonatal). Los neonatos con AAS grave de inicio neonatal generalmente parecen normales durante las primeras 24-48 horas de vida, pero en pocos días presentan hiperamonemia grave que se manifiesta con letargia, somnolencia, rechazo a mamar, vómitos, taquipnea y alcalosis respiratoria. Sin tratamiento, se puede producir un empeoramiento de la letargia, convulsiones, coma y la muerte. La AAS de inicio tardío la desencadena generalmente una infección aguda, estrés o una elevada ingesta proteica. También se han descrito presentaciones como discapacidad cognitiva de inicio tardío o dificultades de aprendizaje, en ausencia de episodios hiperamonémicos. Algunos pacientes pueden ser asintomáticos. Las complicaciones a largo plazo asociadas con ambas formas de AAS incluyen hepatomegalia crónica, disfunción hepática (fibrosis o cirrosis), déficits neurocognitivos (es decir, discapacidad cognitiva, convulsiones y retraso del desarrollo), cabello quebradizo (es decir, tricorrexis nodosa), hipopotasemia e hipertensión arterial.
Etiología
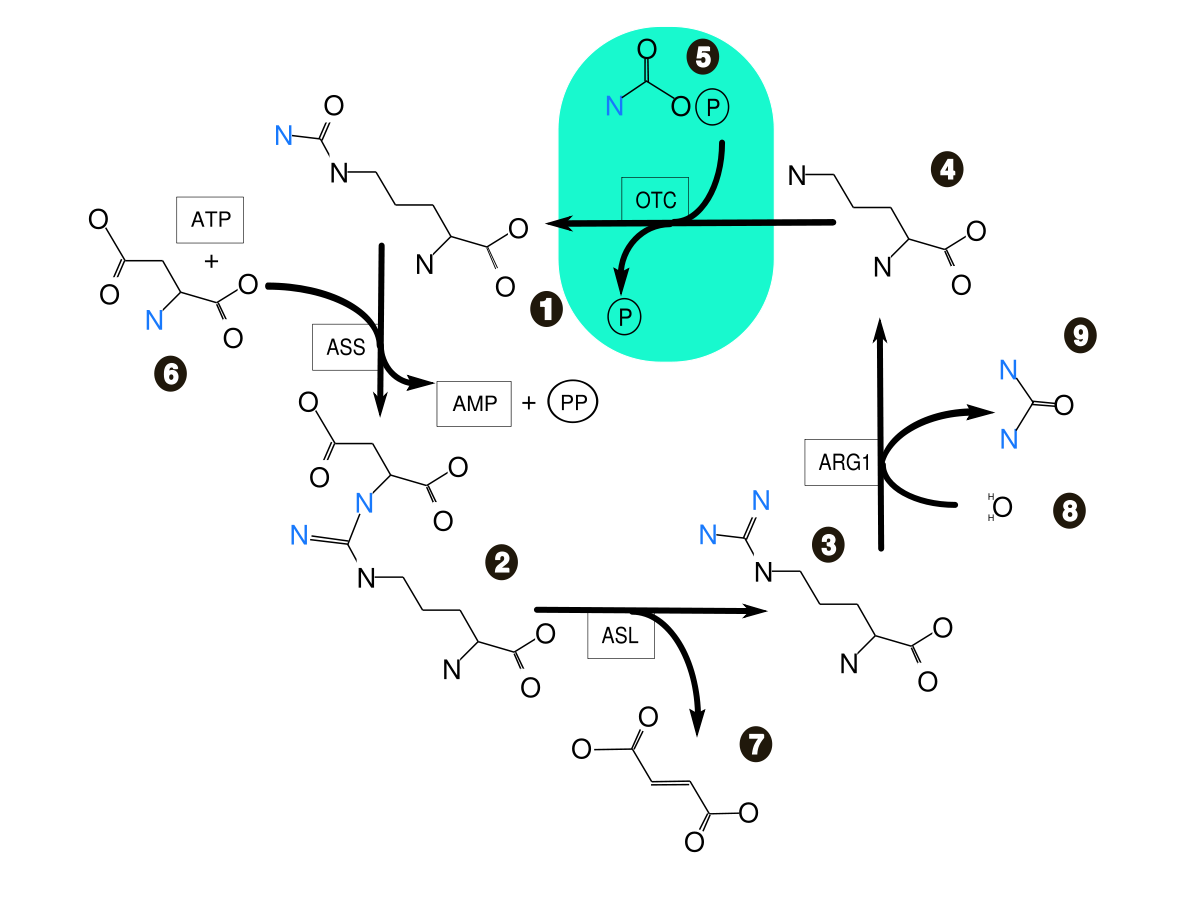
La AAS está causada por mutaciones en el gen ASL (7q11.21) que codifica la enzima argininosuccinato liasa. Esta enzima cataliza la conversión del ácido argininosuccínico en arginina y fumarato durante la cuarta etapa del ciclo de la urea. Los defectos en esta etapa del ciclo de la urea conllevan una acumulación de amonio, ácido argininosuccínico y citrulina en plasma, y de ácido orótico en orina, así como una deficiencia de arginina plasmática.
Métodos diagnósticos
El diagnóstico se basa principalmente en los hallazgos clínicos y las pruebas de laboratorio. Las concentraciones plasmáticas de amonio (>150 µmol/L) y de citrulina (200-300 µmol/L) están elevadas. Los niveles elevados de ácido argininosuccínico (5-110 µmol/L) en plasma y orina tienen valor diagnóstico y las pruebas de genética molecular confirman el diagnóstico. El cribado neonatal para la AAS está disponible en los Estados Unidos y en partes de Australia, y está contemplado en varios países europeos.
Diagnóstico diferencial
El diagnóstico diferencial incluye otros trastornos del ciclo de la urea tales como la deficiencia de carbamoil-fosfato sintetasa 1, la deficiencia de ornitina transcarbamilasa, la citrulinemia tipo I y la deficiencia de arginasa.
Diagnóstico prenatal
El diagnóstico prenatal es posible en familias con mutaciones conocidas causantes de la enfermedad en ambos alelos.
Consejo genético
La AAS sigue un modo de herencia autosómico recesivo. Es recomendable el asesoramiento genético.
Manejo y tratamiento
Durante un episodio hiperamonémico agudo debe evitarse la ingesta de proteína, y se administrarán lípidos, glucosa e insulina (si es necesario) por vía intravenosa (I.V.) para promover el anabolismo. El tratamiento I.V. con eliminadores de nitrógeno (benzoato sódico y/o fenilacetato sódico) debería normalizar los niveles de amonio, pero si no tiene éxito se recomienda la hemodiálisis. El tratamiento a largo plazo incluye una dieta con restricción proteica así como la suplementación de arginina. Para aquellos pacientes con episodios frecuentes de descompensación metabólica o con hiperamonemia incluso cuando siguen una dieta restrictiva en proteína, la administración oral diaria de eliminadores de nitrógeno puede tener éxito. El trasplante hepático ortotópico libera de la hiperamonemia de forma permanente pero no parece ser suficiente para corregir las complicaciones neurológicas. La hipertensión arterial puede ser tratada supliendo la deficiencia de óxido nítrico de esta enfermedad.
Pronóstico
Con un diagnóstico y tratamiento tempranos es posible evitar los episodios hiperamonémicos, pero las complicaciones a largo plazo (discapacidad neurocognitiva, enfermedad hepática e hipertensión arterial) son frecuentes y tienen un efecto negativo sobre la esperanza y calidad de vida.