Estados Unidos:
Kristi Rosa
La
Administración de Drogas y Alimentos de los EE. UU. (FDA) otorgó una
designación de vía rápida al CX-01 de Cantex Pharmaceuticals, Inc. para
el tratamiento de pacientes mayores de 60 años que están recibiendo
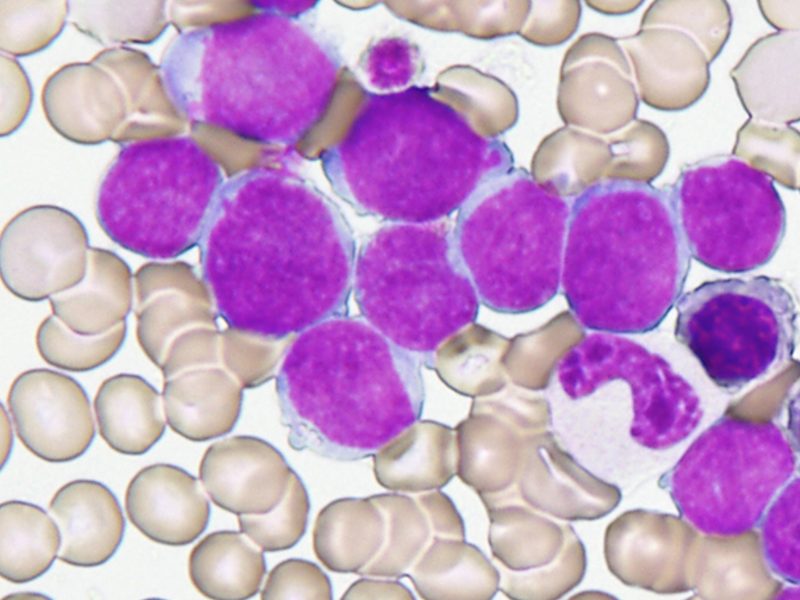
terapia de inducción para la leucemia mieloide aguda recién
diagnosticada (AML)
La AML es la forma más común de leucemia aguda en adultos y se estima que alrededor del 60% de los 19,500 casos proyectados para 2018 ocurrirá en personas mayores de 60 años.
«Más de 60 años, la respuesta a la terapia de ‘inducción’ inicial es menor, el riesgo de recaída es mayor y la supervivencia general es generalmente más corta, lo que crea una necesidad médica significativa insatisfecha para mejorar la efectividad de esta terapia de inducción», Stephen Marcus , MD, director ejecutivo de Cantex, explicó en una declaración reciente. «Creemos que la adjudicación de Fast Track Designation representa el reconocimiento del potencial de CX-01 para abordar una necesidad importante no satisfecha en el tratamiento de la AML mediante la mejora de la eficacia de la quimioterapia de AML de primera línea».
Un polisacárido derivado de una clase de compuestos conocidos como heparinoides, CX-01 ha sido diseñado para «bloquear» la actividad de quimiocinas que estimula la resistencia de los cánceres de sangre al tratamiento disponible y contribuye a la suspensión de la recuperación de médula ósea después de la quimioterapia.
Actualmente, el producto se evalúa en un ensayo aleatorizado de fase 2b en el que los investigadores buscan determinar si la adición de CX-01 a la terapia de consolidación e inducción estándar para AML puede aumentar la eficacia de la terapia de inducción / consolidación en comparación con los pacientes que reciben terapia estándar de inducción / consolidación solo.
El ensayo inscribirá a 75 pacientes mayores de 60 años con LMA recién diagnosticada en varios centros de investigación importantes en todo Estados Unidos. Para el ensayo, los participantes serán aleatorizados en 1 de 3 grupos de tratamiento: aquellos que recibirán terapia de inducción / consolidación estándar solo, aquellos que recibirán terapia estándar de inducción / consolidación con CX-01 a un nivel de dosis más bajo o más alto.
Los participantes recibirán hasta 2 ciclos de inducción y hasta 2 ciclos de consolidación dentro de la prueba de 18 meses. Durante este tiempo, los investigadores realizarán pruebas de laboratorio clínico de rutina y realizarán aspirados de médula ósea y biopsias durante los ciclos de inducción. Monitorearán a los participantes en busca de eventos adversos para determinar la seguridad de la combinación.
La remisión completa morfológica revaluada por los criterios de IWG es el punto final primario del ensayo; esto se evaluará durante las fases de inducción y reinducción del tratamiento, hasta 60 días después del inicio de cada ciclo de tratamiento.
La supervivencia sin complicaciones, la supervivencia libre de leucemia, la supervivencia global, la tasa de remisión completa compuesta, la recuperación de neutrófilos, la recuperación de plaquetas y la tasa de mortalidad a 30 días, 60 días y 90 días se enumeran como medidas de resultado secundarias del ensayo .
Los resultados principales de la prueba se esperan para el cuarto trimestre de 2018.
El medicamento también se está evaluando en un ensayo separado de fase 2 iniciado por el investigador en pacientes con síndrome mielodisplásico. Los representantes de Cantex en la reunión anual de la Sociedad Estadounidense de Oncología Clínica 2018 (ASCO 2018) informaron resultados de primera línea para este ensayo.
Previo a este anuncio, CX-01 recibió una designación de medicamento huérfano de la FDA también para el tratamiento de AML.
Artículos relacionados: leucemia mieloide aguda, ensayo clínico, medicamentos huérfanos
Fuente: https://goo.gl/S5DAeh