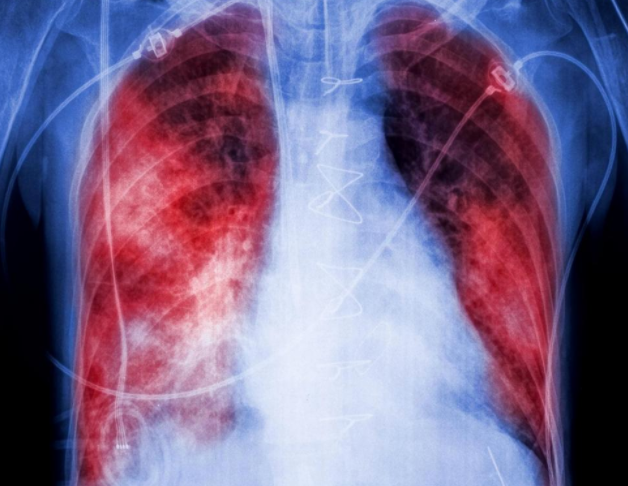
Temprano esta mañana, Reviva Therapeutics anunció que la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) otorgó la designación de fármaco huérfano a su candidata en etapa clínica RP5063, en desarrollo para el tratamiento de la fibrosis pulmonar idiopática (FPI).
La noticia viene después de que se demostró que RP5063 ha demostrado una eficacia robusta en modelos animales de traducción altamente reconocidos que han demostrado emular la fibrosis pulmonar (FP) en humanos.
Los datos de estudios preclínicos muestran que, en los pulmones de modelos animales de PF inducidos por bleomicina, RP5064 mejoró significativamente la tasa de supervivencia, redujo las citoquinas inflamatorias y la cicatrización tisular o fibrosis, lo que indica el potencial del fármaco para una mejoría clínicamente significativa y la estabilización de la función pulmonar.
RP5063, una nueva entidad química (NCE), tiene un nuevo mecanismo de modulación multimodal de las vías de señalización de la serotonina y la dopamina. La señalización de serotonina disfuncional (5-HT) en el pulmón resulta en PF e hipertensión arterial pulmonar (HAP). Se ha demostrado que la señalización de la serotonina que involucra a los receptores 5-HT2A / 2B / 7 del pulmón es vasoconstricción intermedia, remodelación vascular e inflamación vascular, fibrosis y proliferación, todas las cuales son características de la PF y la HAP.
RP5063, es un potente inhibidor de los receptores 5-HT2A / 2B / 7 y, por lo tanto, debilita estos cambios funcionales en una serie de modelos animales probados para imitar las afecciones de PF y HAP en humanos.
«Obtener la designación de medicamento huérfano es un hito reglamentario importante, así como un logro notable para Reviva, ya que valida el potencial terapéutico significativo de RP5063 para el tratamiento de IPF», dijo Laxminarayan Bhat, Ph.D., fundador, presidente y director ejecutivo. de Reviva en un comunicado de prensa. «IPF es una enfermedad devastadora con opciones de tratamiento limitadas y sin cura». RP5063, sin embargo, proporciona un nuevo mecanismo de acción que tiene el potencial de afectar múltiples aspectos de esta enfermedad y, combinado con opciones de entrega convenientes, RP5063 da esperanza a muchos pacientes que sufren de esta enfermedad debilitante «.
En noviembre de 2016, la FDA otorgó la designación de medicamento huérfano a RP5063 para el tratamiento de HAP. Reviva dejó claras sus intenciones de iniciar ensayos clínicos de fase 2 para IPF y HAP en un «futuro muy cercano».
En la actualidad, las opciones de tratamiento para IPF son limitadas y no existe una cura regulada para la afección. Rare Disease Report se encontró con Albert Rizzo, M.D. de la Sección de Medicina Pulmonar y de Cuidados Críticos de Christiana Care en la más reciente Exposición LungFORCE de la American Lung Association (ALA). En el siguiente video, analiza terapias anteriores, actuales y emergentes para la fibrosis pulmonar idiopática.
Artículos relacionados: fibrosis pulmonar idiopática, medicamento huérfano, tratamiento
Fuente: https://goo.gl/PByuGm