Un trabajo de investigación en el Hospital Monte Sinaí de Nueva York, en el que participa Sonia Mulero, investigadora de la Universidad de Extremadura, ha identificado a partir de células madre pluripotentes inducidas una de las proteínas responsable de la hipertrofia cardíaca, un defecto asociado a determinadas enfermedades raras como el síndrome Cardio-Facio-Cutáneo (CFC).
Los resultados, publicados en la revista Stem Cell Reports, pueden ser una opción terapéutica útil para pacientes con hipertrofia cardíaca en síndromes como el cardio-facio-cutáneo u otras etiologías. El síndrome CFC es una enfermedad congénita que forma parte de las denominadas RASopatías, un grupo de enfermedades genéticas raras causadas por la alteración de genes de la ruta de señalización celular RAS/MAPK, de ahí su nombre. En esta ruta de señalización, las mutaciones en el gen BRAF representan el 80% de todos los casos de síndrome CFC.
Los niños afectados por este síndrome tienen problemas cardíacos (malformaciones de las válvulas del corazón, comunicación interauricular y cardiomiopatía hipertrófica), retraso intelectual y de desarrollo, numerosas anomalías cutáneas y rasgos faciales característicos. Su diagnóstico o tratamiento requiere de la intervención multidisciplinar de profesionales debido a la variedad de órganos afectados, y de intervenciones quirúrgicas en el caso de defectos cardíacos.
En la actualidad, y gracias a la detección de mutaciones de los genes afectados, es posible mediante análisis genético realizar un diagnóstico diferencial, aunque la investigación para el tratamiento necesita todavía de mucha colaboración y apoyo social.
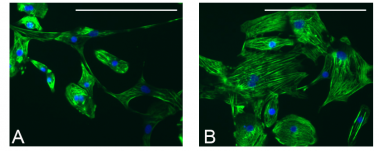
Inmunocitoquímica de cardiomiocitos. Panel A: cardiomiocitos de individuos sanos. Tinción citoplasmática de troponina C (verde) y tinción nuclear con dapi (azul). Panel B: Aumento del tamaño de cardiomiocitos de pacientes con el síndrome cardio-facio-cutáneo. / UEx
Estudio con células madre en cardiopatías
Mulero ha creado un modelo in vitro a partir de células madres pluripotentes inducidas de pacientes con el síndrome CFC y mutaciones en el gen BRAF. El 40% de dichos pacientes desarrollan cardiomiopatía hipertrófica y, por ello, este trabajo ofrece muchas posibilidades en la investigación de dianas terapéuticas de esta enfermedad rara.
“Hemos diferenciado las células madre pluripotentes inducidas humanas de pacientes CFC con mutaciones en el gen BRAF, a células del corazón: cardiomiocitos y fibroblastos, y hemos estudiado los fenotipos de estos dos tipos celulares, así como sus interacciones, que explican la cardiomiopatía hipertrófica, que es uno de los defectos cardíacos más frecuente de estos pacientes”, explica Mulero.
Estos científicos han conseguido descifrar el principal responsable que causa este defecto. “Hemos observado que TGF-beta, una proteína secretada por los fibroblastos, participa en la hipertrofia de los cardiomiocitos. Los fibroblastos diferenciados a partir de las células madres inducidas de los pacientes secretan mayor cantidad de TGB-beta afectando la función normal de los cardiomiocitos. Esto es determinante para la búsqueda de medicamentos que bloqueen la actividad de esta proteína», aclara.